天然牙齿的牙釉质与牙本质是具有各向异性特性的生物材料,其纳米结构在某些区域于牙本质-牙釉质连接处呈现近乎垂直的取向排列,这一独特构造有效阻止了裂缝的扩展。目前的3D剪切诱导打印技术受限于打印方向的单一性,难以完全复制牙齿复杂的三维结构。
东华大学朱美芳院士、张耀鹏研究员受到牙釉质和牙本质纳米结构择优取向的启发,融合了剪切诱导与磁力辅助3D打印技术,开发了一种自下而上的逐步组装策略,构建了具有复杂微观结构的多材料仿生牙冠(图1),该牙冠在不同区域展现出特定的组成成分、性能和优异的生物相容性。相关成果以题为3D Printing of Biological Tooth with Multiple Ordered Hierarchical Structures发表在Materials Toady Bio期刊上,东华大学赵梦露博士为第一作者,耿亚楠硕士、范苏娜副研究员、姚响副研究员和北京化工大学王洁欣教授为共同作者,张耀鹏研究员和朱美芳院士为共同通讯作者。部分实验完成于上海光源BL19U2线站,北京化工大学合作制备了“超重力+”羟基磷灰石。
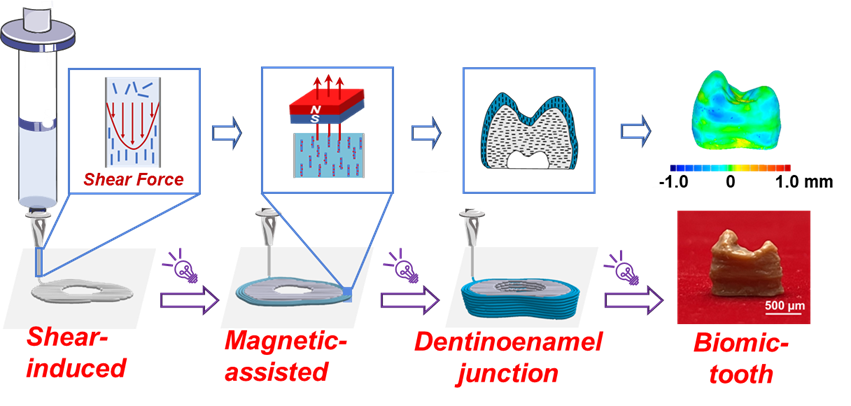
图1. 3D打印多重有序层次结构生物牙齿的示意图
本工作通过静电吸附和高温烧结,对氨基表面改性的HAp纳米棒与SPION@SiO2核壳粉末进行处理,成功赋予了HAp纳米棒磁性特性,并基于此制备了磁响应HAp基齿科修复树脂材料(图2)。通过精确调控磁场方向与强度,实现了对HAp微观排列的精确定向控制(图3)。在牙本质处使用单分散的HAp基树脂,通过剪切诱导使其有序地垂直于牙冠中心轴。在牙釉质处使用磁响应的HAp基树脂,通过磁响应辅助使其平行于牙冠中心轴,其打印精度可达97.9%,并成功仿制了天然牙的硬度梯度(图4)。HAp所释放的钙磷离子可促进人牙髓干细胞的增殖、成骨与分化,为牙体硬组织的再生和龋齿的自我修复提供了理论基础(图5)。此工作为制备具有独特结构和功能的仿生材料提供了新的思路。
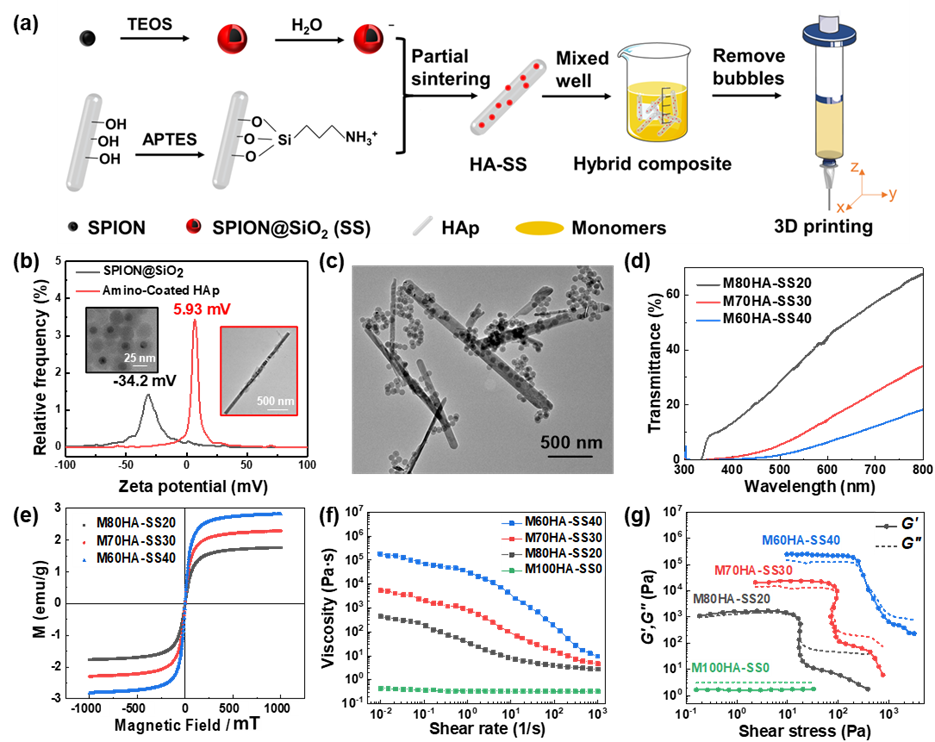
图2. 磁响应HAp基齿科修复树脂墨水的制备及其性能
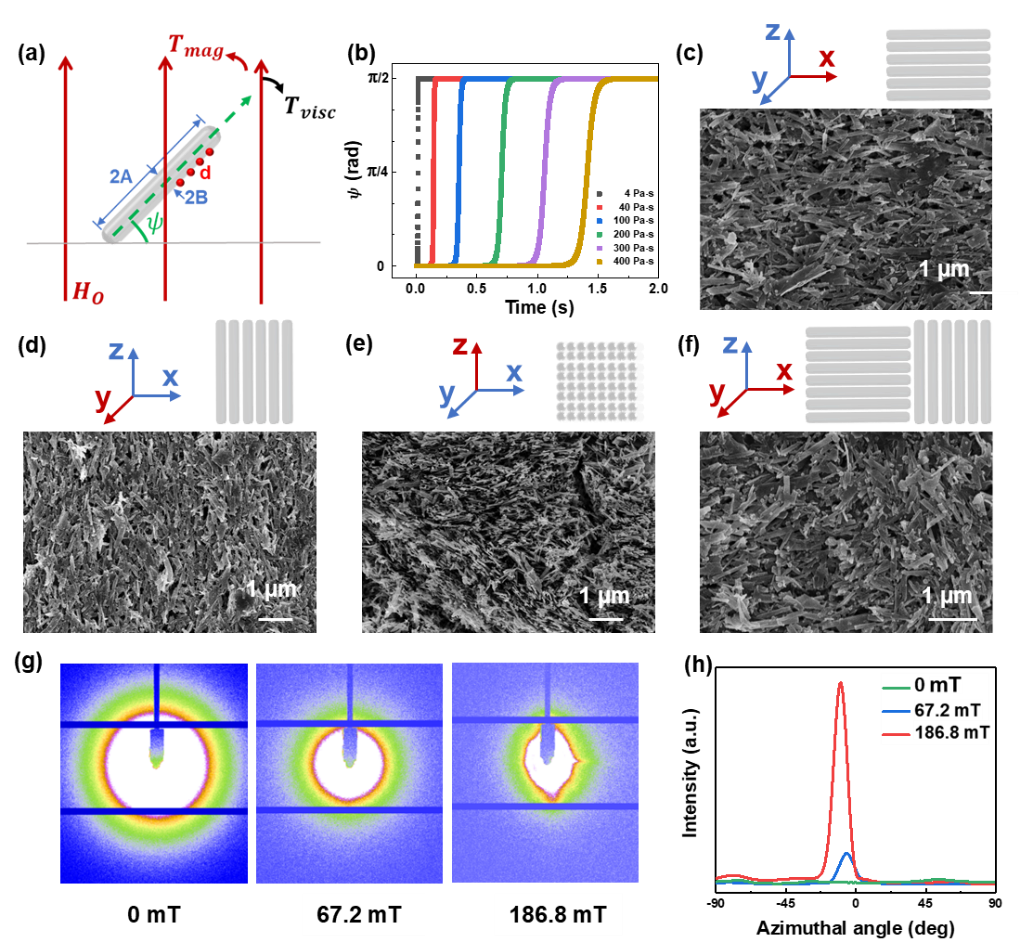
图3. 通过磁力辅助3D打印技术控制HAp纳米棒的微观结构
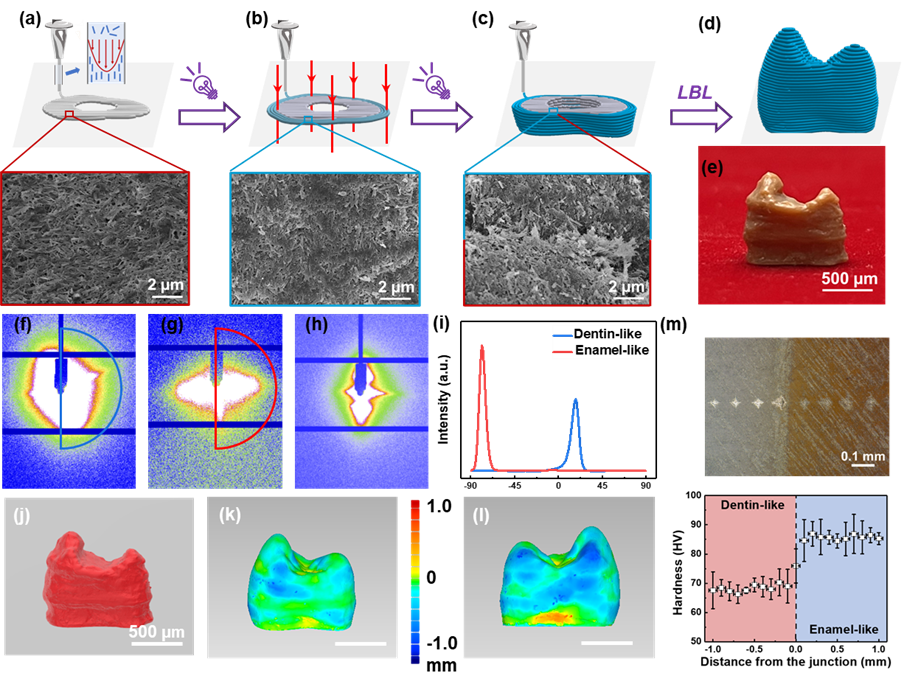
图4. 多材料3D打印牙冠的过程及其性能
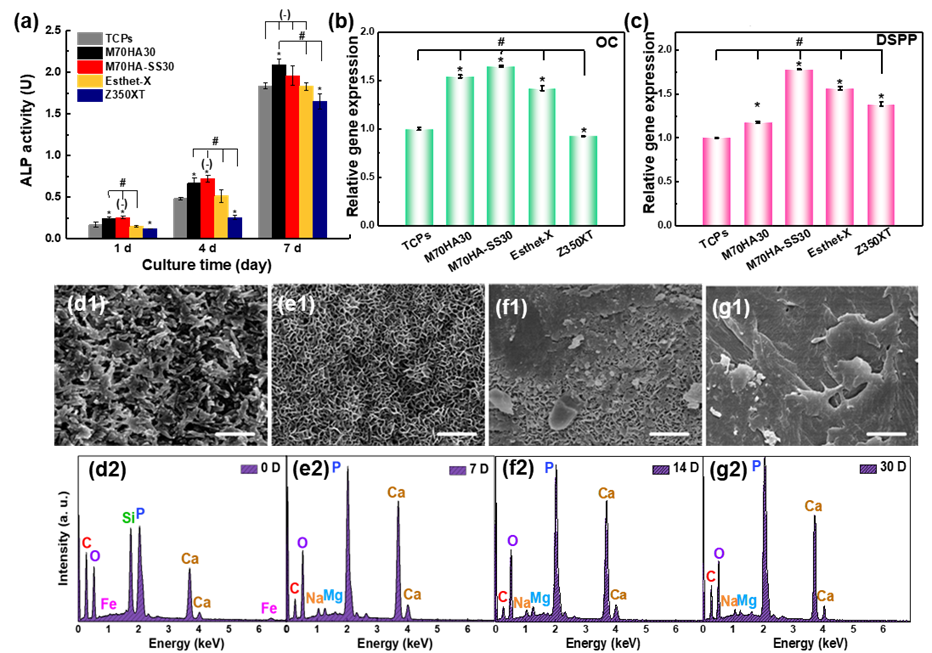
图5. 多材料3D打印齿科树脂的成骨分化及体外生物活性
此工作得到了国家重点研发计划(2016YFA0201702)等项目的资助,以及上海同步辐射光源BL19U2线站、岛津公司在SAXS和Micro-CT测试中提供的支持。